SAL
Una sal es un compuesto químico formado por cationes (iones con carga positiva) enlazados a aniones (iones con carga negativa). Son el producto típico de una reacción química entre una base y un ácido, donde la base proporciona el catión y el ácido el anión.
La combinación química entre un ácido y un hidróxido (base) o un óxido y un hidronio (ácido) origina una sal más agua, lo que se denomina neutralización.
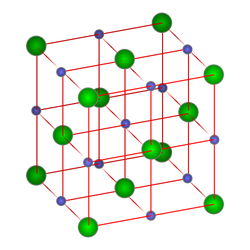
Un ejemplo es la sal de mesa, denominada en el lenguaje coloquial sal común, sal marina o simplemente sal. Es la sal específica cloruro de sodio. Su fórmula molecular es NaCl y es el producto de la base hidróxido sódico(NaOH) y ácido clorhídrico, HCl. En general, las sales son compuestos iónicosque forman cristales. Son generalmente solubles en agua, donde se separan los dos iones. Las sales típicas tienen un punto de fusión alto, baja dureza, y baja compresibilidad. Fundidas o disueltas en agua, conducen la electricidad.
CLASES DE SALES
Los tipos de sales químicas son:
- Neutras ( reacción total de los átomos de hidrógeno del ácido con los oxidrilos del hidróxido), ejemplo: Clorato de Litio: HClO3 + Li(OH)----> Li ClO3 + H20.
- Ácidas o Hidrogenadas ( reacción parcial de los átomos de hidrógeno del ácido con los radicales oxidrilos del hidróxido, los oxácidos que participan deben de poseer como mínimo 2 protones H), ejemplo: Sulfato ácido o hidrógeno de Ca----> 2H2SO4 + Ca(OH)2---> Ca(HSO4)2 + 2 H20.
- Básicas o Alcalinas, poseen grupos (OH) que determinan la alcalinidad o basicidéz de la sal, los hidróxidos que participan deben de poseer 2 o mas gruposd (OH), ejemplo: Nitrato Básico de Aluminio----> 2HNO3 + Al(OH)3----> Al (OH) (NO3)2 + 2 H20.
- Dobles o Mixtas. son aquellas en las que participan 2 hidróxidos combinados con el mismo ácido, ejemplo. Clorito Doble de Calcio y Litio----> 3HClO2 + Ca(OH)2 + Li(OH)----> Ca Li (ClO2)3 + 2 H20.
- Haloideas, Hidrácias o Hidruras: son aquellas sales Binarias en las que solo particpan las ácidos binarios, hidrácido o hidruros No metálicos, por ej: Sullfuro Áurico: 3H2S + 2Au(OH)3----> Au2S3 + 6 H20.
Una sal es un compuesto químico formado por cationes (iones con carga positiva) enlazados a aniones (iones con carga negativa). Son el producto típico de una reacción química entre una base y un ácido, donde la base proporciona el catión y el ácido el anión.
La combinación química entre un ácido y un hidróxido (base) o un óxido y un hidronio (ácido) origina una sal más agua, lo que se denomina neutralización.
Un ejemplo es la sal de mesa, denominada en el lenguaje coloquial sal común, sal marina o simplemente sal. Es la sal específica cloruro de sodio. Su fórmula molecular es NaCl y es el producto de la base hidróxido sódico(NaOH) y ácido clorhídrico, HCl. En general, las sales son compuestos iónicosque forman cristales. Son generalmente solubles en agua, donde se separan los dos iones. Las sales típicas tienen un punto de fusión alto, baja dureza, y baja compresibilidad. Fundidas o disueltas en agua, conducen la electricidad.
CLASES DE SALES
Los tipos de sales químicas son:
- Neutras ( reacción total de los átomos de hidrógeno del ácido con los oxidrilos del hidróxido), ejemplo: Clorato de Litio: HClO3 + Li(OH)----> Li ClO3 + H20.
- Ácidas o Hidrogenadas ( reacción parcial de los átomos de hidrógeno del ácido con los radicales oxidrilos del hidróxido, los oxácidos que participan deben de poseer como mínimo 2 protones H), ejemplo: Sulfato ácido o hidrógeno de Ca----> 2H2SO4 + Ca(OH)2---> Ca(HSO4)2 + 2 H20.
- Básicas o Alcalinas, poseen grupos (OH) que determinan la alcalinidad o basicidéz de la sal, los hidróxidos que participan deben de poseer 2 o mas gruposd (OH), ejemplo: Nitrato Básico de Aluminio----> 2HNO3 + Al(OH)3----> Al (OH) (NO3)2 + 2 H20.
- Dobles o Mixtas. son aquellas en las que participan 2 hidróxidos combinados con el mismo ácido, ejemplo. Clorito Doble de Calcio y Litio----> 3HClO2 + Ca(OH)2 + Li(OH)----> Ca Li (ClO2)3 + 2 H20.
- Haloideas, Hidrácias o Hidruras: son aquellas sales Binarias en las que solo particpan las ácidos binarios, hidrácido o hidruros No metálicos, por ej: Sullfuro Áurico: 3H2S + 2Au(OH)3----> Au2S3 + 6 H20.
